Schock
Ultraschall in der Notfallmedizin
Dr. med. Konstantin Schraepler, Bremen 09/2023
Pathophysiologie
Schock: Pathophysiologie
vereinfacht:
Kreislaufversagen, das zur Minderperfusion der Organe mit unzureichender O2-Versorgung und dadurch zur Funktionsstörung führt
Standl T et al. (2018) Dtsch Arztebl Int 115:757-768
Schock: Einteilung anhand der Hämodynamik
- eingeschränktes Herzzeitvolumen: Low output -Versagen
- ➡ hoher systemischer Gefäßwiderstand, hohe avDO2
- erhöhtes Herzzeitvolumen: High output -Versagen
- ➡ niedriger systemischer Gefäßwiderstand, geringe avDO2
Filippatos G et Zannad F (2007) Heart Fail Rev 12:87-90
Gheorghiade M et al. (2005) Circulation 112:3958-3968
Hollenberg SM et al. (1999) Ann Intern Med 131:47-59
Yancy CW et al. (2013) Circulation 128:e240-327
Schock: Einteilung anhand der Hämodynamik
- eingeschränktes Herzzeitvolumen: Low output -Versagen
- ➡ hoher systemischer Gefäßwiderstand, hohe avDO2
- Einteilung anhand LV-Funktion
- mit reduzierter LV-Funktion
- mit erhaltener LV-Funktion
- ➡ niedriger systemischer Gefäßwiderstand, geringe avDO2
Filippatos G et Zannad F (2007) Heart Fail Rev 12:87-90
Gheorghiade M et al. (2005) Circulation 112:3958-3968
Hollenberg SM et al. (1999) Ann Intern Med 131:47-59
Yancy CW et al. (2013) Circulation 128:e240-327
Schock: Einteilung anhand der Hämodynamik
- eingeschränktes Herzzeitvolumen: Low output -Versagen
- mit reduzierter LV-Funktion
- Myokardinfarkt
- großer Infarkt, kleinerer Infarkt bei vorbestehender LV-Dysfunktion, Re-Infarkt, Infarktausdehnung
- Endstadium Kardiomyopathie
- Myokarditis
- Myokardkontusion
- septische Kardiomyopathie
- Myokardinfarkt
- mit erhaltener LV-Funktion
- Klappenvitien
- rechtsventrikuläre Dysfunktion
- Heart Failure with preserved Ejection Fraction [HFpEF]
- Perikardtamponade
- Hypovolämie
- mit reduzierter LV-Funktion
- erhöhtes Herzzeitvolumen: High output -Versagen
-
- distributiver Schock (Verteilungsschock)
- Septischer Schock
- Anaphylaktischer Schock
- Anämie
- Hypervolämie
- Thyreotoxikose
- arteriovenöse Fisteln
- Leberzirrhose
- etc.
- distributiver Schock (Verteilungsschock)
-
Filippatos G et Zannad F (2007) Heart Fail Rev 12:87-90
Gheorghiade M et al. (2005) Circulation 112:3958-3968
Hollenberg SM et al. (1999) Ann Intern Med 131:47-59
Yancy CW et al. (2013) Circulation 128:e240-327
die technik
wieviel Schnittebenen?
wenig Rüstzeug
viel Aussage
Kompromiss: Minimal-Schnittebenen vs. Aussagekraft
- subkostale Schnitte
- subkostale lange Achse
- subkostaler 4-Kammerblick
- subkostale kurze Achse
- apikale Schnitte
- 4-Kammerblick/ 5-Kammerblick
- 2-Kammerblick
- 3-Kammerblick
- parasternale Schnitte
- lange Achse
- kurze Achse
Jensen MB et al. (2004) Eur Anaesthesiol 21:700-707
Labovitz et al. (2010) Am Soc Echocardiogr 23:1225-1230
Mitchell C et al.(2019) J Am Soc Echocardiogr 32:1-64
Kompromiss: Minimal-Schnittebenen vs. Aussagekraft
- subkostale Schnitte
- subkostale lange Achse
- subkostal 4-Kammerblick
- apikale Schnitte
- 4-Kammerblick/ 5-Kammerblick
-
der Untersuchungsablauf (immer der gleiche)
- subkostale Schnitte ➡ Rückenlage
- subkostaler 4-Kammerblick
- hämodynamisch wirksamer Perikarderguß?
- Ersteinschätzung LV- und RV-Funktion
- subkostale lange Achse:
- Beurteilung Volumenstatus
- subkostaler 4-Kammerblick
- apikale Schnitte ➡ Linksseitenlage erleichtert Darstellung
- apikaler 4-Kammerblick
- Beurteilung LV- und RV-Funktion
- Beurteilung MV-/ TV-Funktion
- apikaler 5-Kammerblick
- Beurteilung AoV-Funktion
- Beurteilung Hämodynamik
- apikaler 4-Kammerblick
subkostale Schnitte
Einstellung der subkostalen Schnitte

subkostaler
4-Kammerblick

subkostaler 4-Kammerblick
Mitchell C et al.(2019) J Am Soc Echocardiogr 32:1-64Perikarderguss?
Perikarderguss
- echofreier/-armer Raum zwischen Epikard und Perikard
- ab ca. 15-35 ml erkennbar
- Dynamik des Auftretens entscheidet über die hämodynamische Relevanz
- akuter Perikarderguß: ≥50 ml hämodynamische Instabilität
- chronischer Perikarderguß: Toleranz bis zu 2000 ml
- typisches morphologisches Korrelat: swinging heart
- hämodynamische Relevanz ergibt sich aus:
- primär typischer Klinik
- obere Einflussstauung, Hypotonie, Tachykardie, Pulsus paradoxus
- Bildgebung sekundär
- primär typischer Klinik
- Perikardiozentese-Zugang im Notfall primär von subkostal
hämodynamische Relevanz in der Bildgebung
- Kollaps der Herzhöhlen
- Ablauf der Beeinträchtigung: RA (initial systolisch) ➙RV (initial diastolisch) ➙LV
- V. cava inferior dilatiert
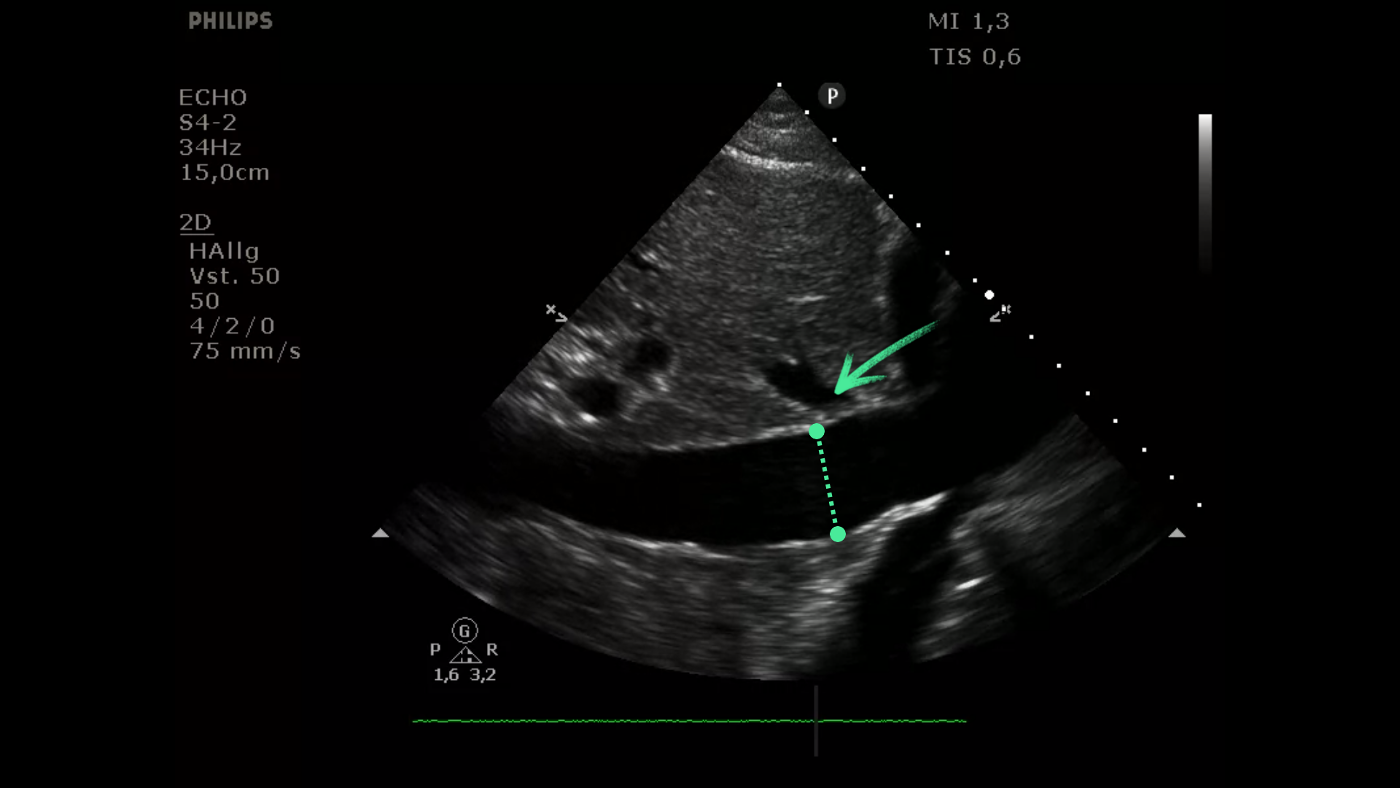
Schock nach Herzkatheter
Echofreier Raum zwischen Epikard und Perikard mit Kollaps des rechten Ventrikels
Hypotonie
Auffällige Hypotonie bei ansonsten weitgehend asymptomatischen Patienten mit neutropener Enterokolitis. Tamponierender hämorrhagischer Perikarderguss. Kollaps des rechten Vorhofs und Ventrikels.
Primär-Einschätzung
LV-/ RV-Funktion
Primär-Einschätzung LV-/ RV-Funktion
- nur grobe Beurteilung
- schiefe Anschnitte erschweren die Interpretation
- Beachtung des interatrialen Septums
- Auslenkung in den linken Vorhof ➡ rechtsatrale Drücke übersteigen die linksatrialen
Reanimation
Reanimation bei Kammerflattern (EKG!). Eine Perikardtamponade ist auszuschließen. Es zeigt sich ein hämodynamisch nicht relevanter Perikarderguß.
kreislaufinstabil, febril
Septischer Schock. Hyperdynam erscheinender rechter und linker Ventrikel, aber die bei der Patientin bestehende Sinustachykardie von 130/min. kann eine ausreichende Pumpfunktion vortäuschen. Die Ventrikel wirken beidseits ausreichend gefüllt. Es besteht ein hämodynamisch nicht relevanter Perikarderguß.
hämodynamische Instabilität, Dyspnoe
Akute Lungenarterienembolie. Flottierender Thrombus im rechten Vorhof und Wölbung des rechten Vorhofs in den linken Vorhof als Zeichen der rechtsatrialen Druckerhöhung.
subkostale
lange Achse
subkostale lange Achse

Volumenstatus
Darstellung in 2 Ebenen:
lange und kurze Achse
Kircher BJ (1990) Am J Cardiol 66:493–496
Milli M, Inferior and Superior Venae Cavae. In: Sarti A, Lorini FL, editors. Echocardiography for Intensivists, Springer 2009; 121-124
diagnostischer Algorithmus
diagnostischer Algorithmus der Bestimmung des Volumenstatus geht direkt in die Therapiesteuerung über
 nach Paul Mayo, ISICEM 2014
nach Paul Mayo, ISICEM 2014Methodik
Messung end-exspiratorisch senkrecht der langen Achse direkt proximal Einmündung der Lebervenen (ca. 0,5 bis 3,0 cm proximal Ostium rechter Vorhofs)
Wer benötigt Volumen?
wenn Kaliberschwankungen bzw. kollabierend: Volumengabe!
Kircher BJ (1990) Am J Cardiol 66:493–496
Milli M, Inferior and Superior Venae Cavae. In: Sarti A, Lorini FL, editors. Echocardiography for Intensivists, Springer 2009; 121-124
Bewertung der V. Cava inferior-Weite
- zur Abschätzung des Volumenstatus nur ein Baustein
- erfolgt qualitativ anhand:
- des Durchmessers und der inspiratorischen Kaliberveränderung
- dynamische Bewertung (= VCI-Kollapsibilität) korreliert stärker mit intravaskulärem Volumenstatus als einzelne statische Diametermessungen
- VCI-Kollapsibilität >50% entspricht RAP von <5 mmHg
- VCI-Kollapsibilität = VCI-Durchmessermaximal / VCI-Durchmesserminimal x 100
- für beatmete Patienten bisher keine ausreichend validen physiologischen IVC-Parameter (Größe, Kollapsibilität, Dehnbarkeit) definiert
- des Durchmessers und der inspiratorischen Kaliberveränderung
Seif D (2012) J Ultrasound Med 2012; 31:1885–1890
Rudski LG (2010) J Am Soc Echocardiogr 23:685-713
Wer benötigt Volumen?
wenn linker/ rechter Ventrikel hyperdynam und Kissing walls: Volumengabe!
apikale Schnitte
Einstellung apikale Schnitte

apikaler
4-Kammerblick

apikaler 4-Kammerblick
Mitchell C et al.(2019) J Am Soc Echocardiogr 32:1-64visuelle Bewertung
Tachypnoe, SaO2 89% bei Raumluft
Dekompensierte Herzinsuffiziez. Einschränkung der linksventrikulären Pumpfunktion mit Dyskinesie des Septumbereichs.
Dyspnoe, Hypotonie, Katecholamin-pflichtig
Endstadium kardiale AL-Amyloidose. Deutliche Verdickung des Myokards mit auffälliger grobscholliger Textur. Vergrößerung beider Vorhöfe. Deutlich erkennbare Einschränkung der linksventriulären Pumpfunktion.
hypoton, tachykard, Lactatämie
Tamponierender Perikarderguss mit Kollaps des rechten Vorhofs und Ventrikels.
kreislaufinstabil, vor 3 Tagen Brustschmerz
Subakuter Myokardinfarkt, Konturunterbrechung des medialen Septums bei Ventrikelseptumdefekt (Komplikation Myokardinfarkt).
febril, hypoton
TV-Endokarditis. Große, flottierende, dem Trikuspidalsegel anhaftende Vegetation.
hypoton, dyspnoisch, Schüttelfrost
LVFTs-Endokarditis. Große, frei flottierende Struktur im linken Ventrikel einer Linksventrikulären falschen Sehne (Left ventricular false tendons [LVFTs], aberranter Sehnenfaden)
Pumpfunktion
Aufschlüsselung Pumpfunktion
- systolische Funktion
- radiale Funktion
- longitudinale Funktion
- torsionale Funktion
- diastolische Funktion
viele Methoden der Bestimmung
- linker Ventrikel:
- Ejektionsfraktion (EF)
- MAPSE
- Shortening fraction (Diameter, Fläche)
- ߡp/ߡt
- Cardiac power
- annular systolic velocity
- venticular longitudinal systolic strain
- Speckle tracking
- rechter Ventrikel:
- TAPSE
- FAC
- venticular longitudinal systolic strain
LV-Funktion
Ejektionsfraktion (EF)
Was ist die EF?
- = prozentueller Anteil des Schlagvolumens am enddiastolischem Ventrikelvolumen
- bzw. EF = (Volumenenddiastolisch - Volumenendsytolisch) / Volumenenddiastolisch x 100
echokardiographische EF-Bestimmung:
- nach Simpson:
- zwei-dimensional
- drei-dimensional
- nach Teichholz bzw. Quinones
- nach Dumesnil
Lang RM et al. (2015) J Am Soc Echocardiogr 28:1-39
Quinones MA et al. (1981) 64:744-753
Teichholz LE et al. (1976) Am J Cardiol 37:7-11
Allgemeines zur EF-Bestimmung nach Simpson:
- Voraussetzung: gute Visualisierung des Endokards
- schlechte Schallqualität in 23–31% d.F. bei denen die EF nicht planimetriert werden kann
- bei beatmeten, hämodynamisch instabilen kritisch Kranken
nur eingeschränkte Anwend- und Reproduzierbarkeit
Robotham JL et al. (1991) Anesthesiology 74:172-183
einfacher, schneller?
was interessiert?
- die eingeschränkte = nichterhaltende systolische LV-Funktion
= abnormale systolische LV-Funktion!
➙ d. h. EF <50%
Eyeball (EBEF)
Tipp: beachte die Exkursionen der Mitralklappenebene
Frage: EBEF > 50%?
Die EF beträgt >50%. Gut ist neben der Verschmälerung (radiale Funktion) die Verkürzung (longitudinale Funktion) des linken Ventrikels zu erkennen.
Frage: EBEF > 50%?
die EF beträgt <50%. Auffällig sind die verminderten Exkursionen des Mitralanulus über den Herzyklus (s. MAPSE). Diese longitudinale Funktion ist wesentlicher Bestandteil der linksventrikulären Pumpfunktion und visuell besser als die EF zu erfassen. Der Abstand zwischen den Punkten des Messkursurs ist 1 cm. Ausgemessen nach Simpson liegt die EF bei 20%.
Frage: EBEF > 50%?
die EF beträgt >50% bei hyperdynamer linksventrikulärer Funktion
Frage: EBEF > 50%?
Die EF beträgt <50%. Auffällig ist die verminderten Exkursionenen des Mitralanulus über den Herzyklus (s. MAPSE). Diese longitudinale Funktion ist wesentlicher Bestandteil der linksventrikulären Pumpfunktion und visuell besser als die EF zu erfassen. Ausgemessen nach Simpson lag die LV-Funktion bei 40%.
Frage: EBEF > 50%?
Die EF beträgt <50%. Auch hier ist verminderte longitudinale Funktion visuell sehr gut zu erfassen. Ausgemessen nach Simpson lag die LV-Funktion bei 35%.
Nachteile der EF:
- große Inter- und Intraobservervariabilität
- EF-Änderungen <10% nicht unbedingt tatsächliche Veränderung der systolischen Funktion
- meist als wesentlicher LV-Funktionsparameter angesehen - was sie nicht ist!!
- Abhängigkeit Vorlast, Nachlast und Herzfrequenz
- kein direktes Maß der Kontraktilität
Muraru D et al. (2014) 27:1025-1028
Pellikka PA et al. (2018) JAMA Netw Open 1:e181456
Thavendiranathan P et al. (2013) J Am Soc Echocardiogr 26:1267-12
einfach, besser?
MAPSE
Mitral Annular Plane Systolic Excursion (MAPSE)
früher: AVPD
Atrioventricular Plane Deviation (AVPD)
Hu K (2012) Eur H J Cardiovasc Imaging 14:205-212Die Messung der MAPSE erfolgt an zwei Regionen. Die MAPSElateral wird am lateralen Mitralklappenannulus unter Verwendung der Zoomfunktion mittels M-Mode bestimmt.
Die Messung erfolgt vom tiefsten Punkt der Enddiastole bis zum Ende der T-Welle (=Aortenklappenschluß) = genau genommen entspricht sie nicht exakt der maximalen Mitralringexkursion.
Die MAPSEseptal wird am septalen Mitralklappenannulus bestimmt. Die MAPSEseptal ist physiologischerweise etwas geringer als die MAPSElateral.
Allgemeines zur MAPSE
- auch bei ungeübten Untersuchern sehr präziser Prädiktor der globalen LV-Funktion
- korrelliert bei systolischem Pumpversagen mit der Ejektionsfration
Männer : EF = 4.8 x MAPSE + 5.8
Frauen : EF = 4.2 x MAPSE + 20
näherungsweise:
EF (in %) = 5x MAPSE (in mm) + 5
- MAPSE (= longitudinale Funktion) macht ca. 60% des Schlagvolumens aus
- spiegelt systolische und auch diastolische LV-Funktion wider
- direkter, früher, empfindlicher Parameter der systolischen longitudinalen LV-Dysfunktion
Zaca V (2010) Heart Fail Rev 15:23–37
Quantifizierung der linksventrikulären systolischen Funktion
| LV-Einschränkung | keine | leicht | moderat | schwer | |
| EF (%) | ♀>53/♂>51% | 41-♀53/♂51% | 30-40 | <30 | |
| MAPSE (mm) | ≥11 | 9-10 | 6-8 | <6 |
Zaca V (2010) Heart Fail Rev 15:23–37
RV-Funktion
Ursachen akutes Rechtsherzversagen
- akute Lungenarterienembolie
- dekompensiertes chronisches Cor pulmonale
- rechtsventrikulärer Myokardinfarkt
Merkmale rechtsventrikuläre Dysfunktion
- Dilatation
- Druckerhöhung
- Hypokinesie
Rudski LG (2010) J Am Soc Echocardiogr 23:685-713
RV-Dilatation
rechtsventrikuläre Dilatation
Akute Lungenembolie bei hämodynamisch instabilen Patienten. Typisch ist die Aufweitung des rechten Ventrikels vorallem im mittleren Segment. Ansicht im subkostalen 4-Kammerblick.
- RVD/LVD: <1
rechtsventrikuläre Dilatation
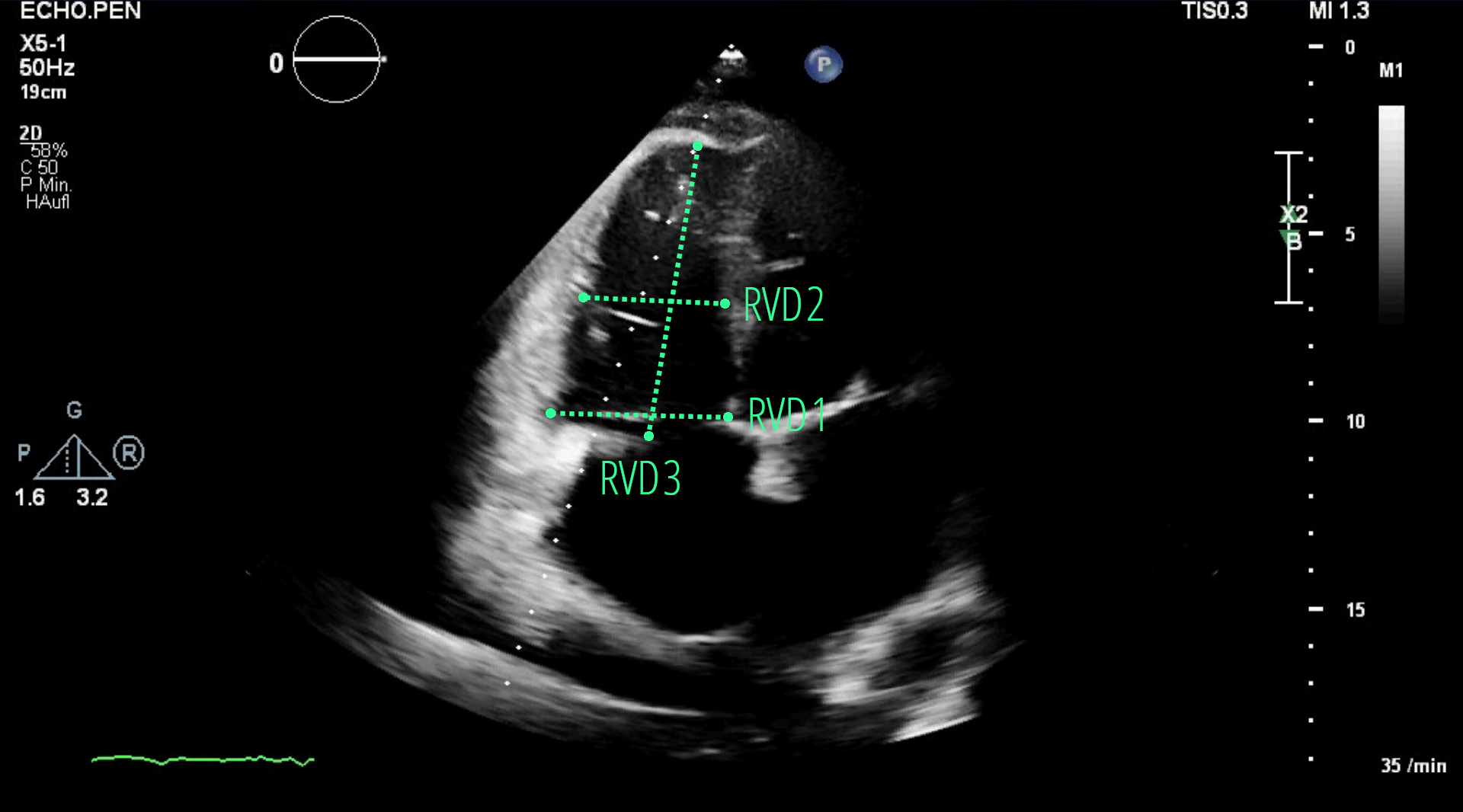
- RVD1<42 mm
- RVD2<35 mm
- RVD3 <86 mm
RV-Druckerhöhung
rechtsventrikuläre Druckerhöhung
nicht-vorerkrankter RV kann einen maximalen PAmean von 40 mmHg kompensieren
- pulmonale Hypertension:
- rechtsventrikulärer-rechtsatrialer Gradient >30 mmHg
- erhöhte Flußgeschwindigkeit über TV >2,8 m/s
- paradoxe Septumkinetik
*für die weitere spezifische Untersuchung (wie z.B. 60/60-Sign, D-shape, linksventrikulärer Exzentritätsindex pulmonale Akzelerationszeit) wären weitere Schnittebenen (parasternal und subkostale kurze Achse etc.) notwendig
Matthews JC et McLaughlin V (2008) Current Cardiol Rev. 4:49–59Rudski LG (2010) J Am Soc Echocardiogr 23:685-713
rechtsventrikuläre Druckerhöhung
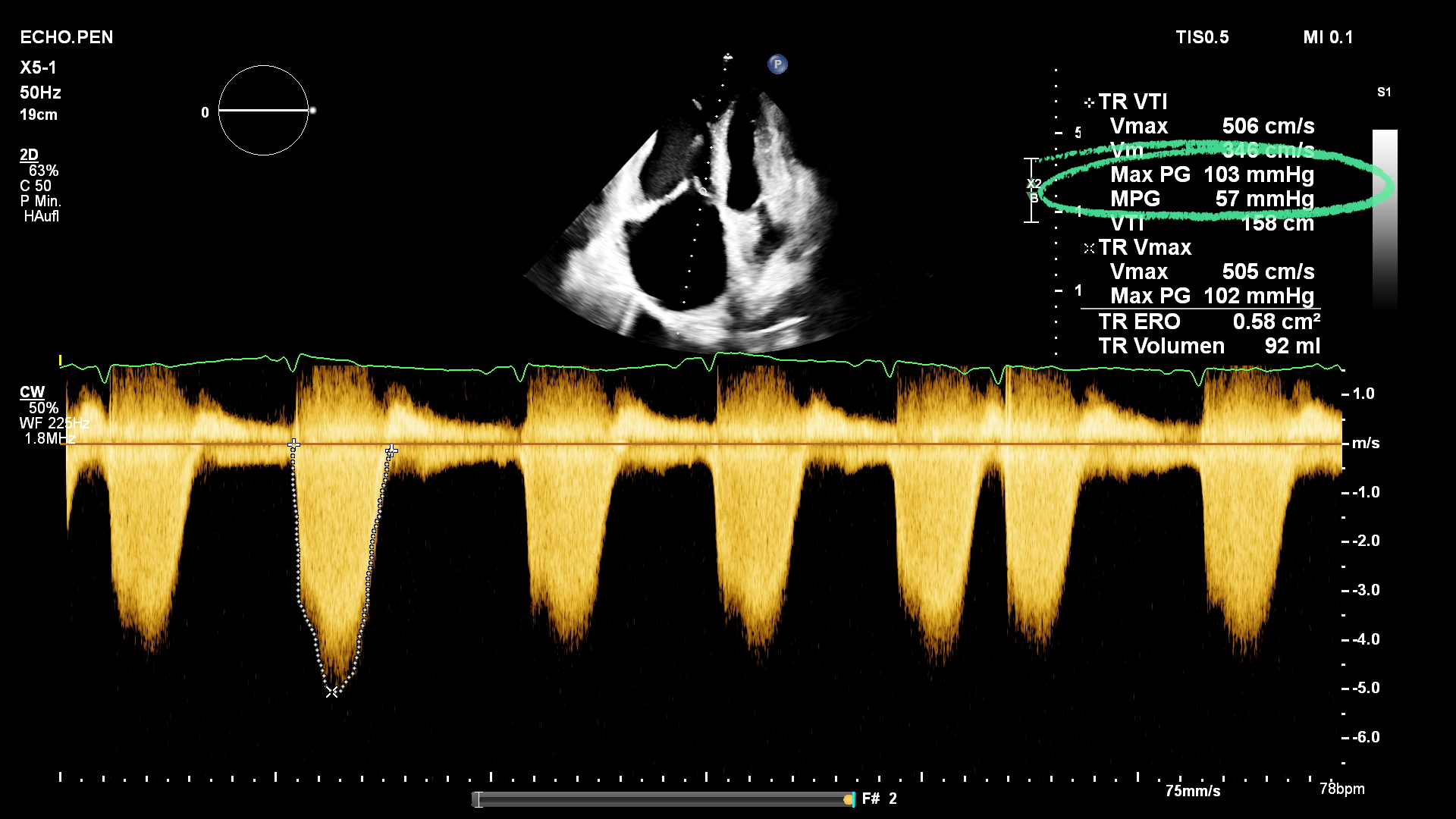
- PAPsyst. max = 4(TRvelocity)2 + RAP
paradoxe Septumbewegung bei RV-Druckerhöhung
Die paradoxe Septumbewegung ist bei RV-Druckerhöhung häufig nur bei viel Übung sofort zu erkannen. Das gesamte Ausmaß der rechtsventrikulären Druckbelastung wärein der parasternalenkurzen Achse leichter zu sehen.
RV-Hypokinesie
rechtsventrikuläre Hypokinesie
Subakuter Rechtsherzinfarkt mit kardiogenem Schock. Auffällig ist die fehlende Kontraktion und Wanddickenzunahme der freien rechtsventrikulären Wand im subkostalen 4-Kammerblick.
rechtsventrikuläre Hypokinesie
Akut dekompensiertes chronisches Cor pulmonale bei schwerer Pulmonal arterieller Hypertonie WHO I mit kardiogenem Schock. Auffällig ist auch hier die fehlende Kontraktion und Wanddickenzunahme der freien rechtsventrikulären Wand im auf den rechten Ventrikel fokussierten apikalen 4-Kammerblick.
rechtsventrikuläre Hypokinesie
- tricuspid annulare plane systolic excursion (TAPSE)
- Zeichen der akuten/ chronischen RV-Dysfunktion
- Normwert >19 mm
- rechtsventrikuläre Dysfunktion <16 mm
- positives McConnell Sign:
- Zeichen der akuten Rechtsherzbelastung
- Sensitivität 77%, Spezifität 94%
- positiv prädiktiver Wert 71%, negativ prädiktiver Wert 96%
Rudski LG (2010) J Am Soc Echocardiogr 23:685-713
TAPSE
Tricuspidal Annular Plane Systolic Excursion (TAPSE)
Matthews JC et McLaughlin V (2008) Current Cardiol Rev. 4:49–59Rudski LG (2010) J Am Soc Echocardiogr 23:685-713
Die Bestimmung der TAPSE erfolgt wie die MAPSE im apikalen 4-Kammerblick unter zur Hilfenahme des M-Mode.
RV
RA
LV
LA
Rudski LG (2010) J Am Soc Echocardiogr 23:685-713Die Messung der TAPSE erfolgt im Bereich der freien rechtsventrikulären Wand am lateralen Trikuspidalklappenannulus unter Verwendung der Zoomfunktion mittels M-Mode.
Die Messung erfolgt vom tiefsten bis zum höchsten Punkt der Trikuspidalringringexkursion.
TAPSE
| RV-Dysfunktion | keine | grenzwertig | leicht | moderat | schwer |
| TAPSE in mm | >19 | 16-19 | 11-15 | 6-10 | <6 |
McConnel-Sign
Akutes Cor pulmonale bei Lungenarterienembolie mit aufgrund des kräftigeren Septums erhaltener Apexkontraktion mit Dyskinesie der schwachen medioapikalen rechtsventrikulären Wand (= McConnel-Sign).
Klappenvitien
Beurteilung von Vitien in der Akutmedizin
- immer Einbeziehung der Klinik
- Beurteilung der Klappen anhand der Morphologie und Beweglichkeit
- ausführliche Doppleruntersuchungen mit Schweregradbeurteilung nicht notwendig
in der Akutmedizin relevante Vitien
- dekompensierte chronische Klappenvitien
- sind Klappeninsuffizienzen und -stenosen
- vorhandene Anpassungsvorgänge
- akute Klappenvitien
- sind Klappeninsuffizienzen (MV-Insuffizienz!)
- keine Anpassungsvorgänge
dekompensierte chronische Klappenstenosen
- typischer Auskultationsbefund
- visuell eingeschränkte Klappenseparation
- verstärkte Sklerosierung
- sekundäre Folgen:
- LV-Hypertrophie bei Aortenklappenstenose
- linksatriale Dilatation bei Mitralklappenstenose
Schmidt J (2012) Med Klin Intensivmed Notfmed 107:571-583
MV-Stenose
Dekompensierte schwere Mitralklappenstenose bei einer Patientin mit anamnestisch rheumatischem Fieber. Es zeigen sich verplumpte Mitralsegel, die verklebt erscheinen bzw. eine deutlich verminderte Separation aufweisen und sich in der Diastole kuppelförmig in den linken Ventrikel wölben (= Leaflet Doming). Erweiterung des linken Vorhofs. Die weitere Evaluation würde mittels pW-Doppler erfolgen.
apikaler
5-Kammerblick
apikaler 5-Kammerblick

AoV-Stenose
Erstdiagnose einer schweren Aortenklappenstenose mit verminderter Separation der ausgeprägt sklerosierten Klappen bei einem Hämodialyse-Patienten mit in den letzten Tagen progredienter Dyspnoe. Die weitere Evaluation erfolgt mittels Dopplersonografie.
cw-Doppler: AoV-Stenose

Darstellung der AoV-Stenose im cw-Doppler.
dekompensierte chronische Klappeninsuffizienzen
- Darstellung Insuffizienzvitien mittels Farbdopplerechokardiographie
- zur Graduierung:
- Abschätzung der Regurgitationsfläche (z.B. bezogen auf die Vorhofgröße)
- Bestimmung der proximalen Jetbreite (Vena contracta)
- Pixeldichte des cw-Doppler-Signals bei der MV-Insuffizienz
- genaue Bestimmung des Schweregrades für die Akutmedizin zu umfangreich
Vena contracta
= kleinster Durchmesser des Insuffizienzjets
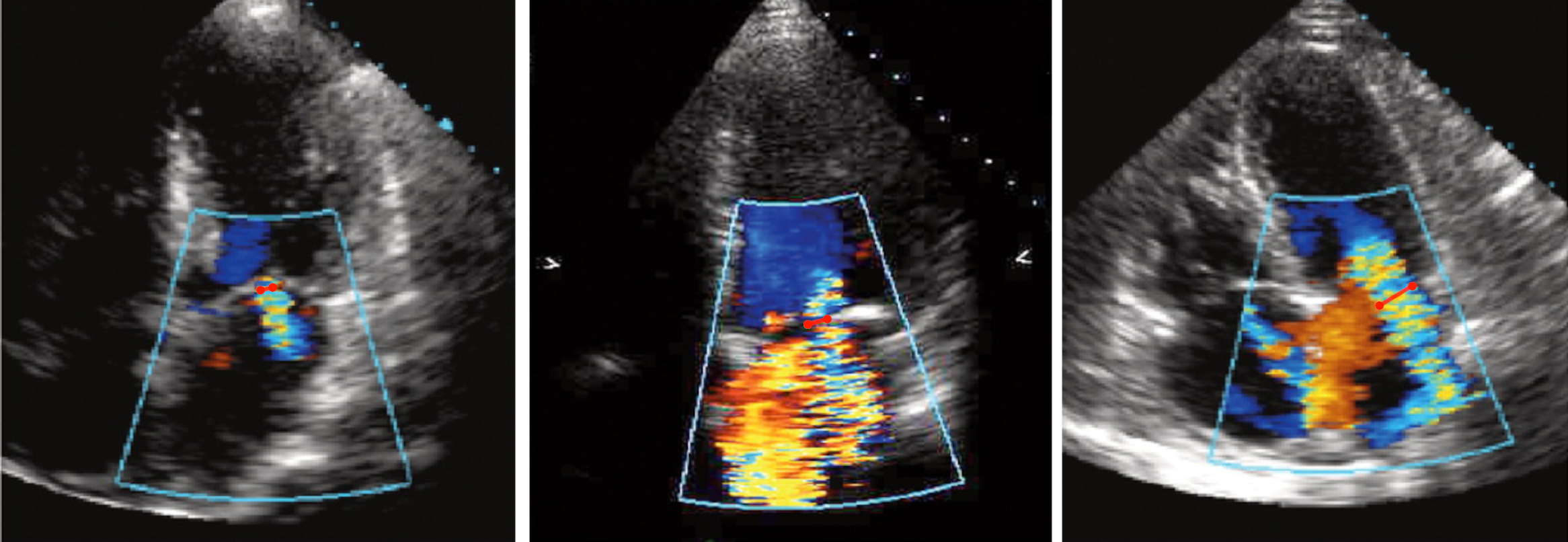
- AoV, MV und TV-Insuffizienz
- <3 mm : leicht
- 3-6 mm : moderat
- ≥7 mm : schwer
Zoghbi WA et al. (2017) J Am Soc Echocardiogr 30:303-371
MV-Insuffizienz
60 jährige Patientin mit rezidivierender Angina pectoris-Symptomatik bei bekannter koronarer Herzkrankheit. Echokardiographisch zeigt sich gegenüber der Voruntersuchung eine signifikante Abnahme der linksventrikulären Pumpfunktion (EF 23%).
MV-Insuffizienz
26 jährige Patientin mit Z.n. Mitralklappenrekonstruktion bei rheumatischer Herzerkrankung und jetzt progredienter Dyspnoe. Die Patientin war nicht mehr in der Lage 1 Etage Treppen zu steigen.
schwere Mitralinsuffizienz

Die erhöhter Densität der Insuffizienzhüllkurve kann als Hinweis auf eine schwere Mitralinsuffizienz dienen. Sie ähnelt dem einer Aortenklappenstenose, unterscheidet sich aber durch den unmittelbaren Beginn nach dem diastolischen Mitralsignal
MV-Insuffizienz II°:
geringere Densität
Tricuspidalinsuffizienz
mittelschwere Trikuspidalinsuffizienz
akute Klappeninsuffizienzen
- in der Akutsituation LV-Funktion zunächst erhalten
- hochturbulenter (mosaikfarbenen) Regurgitationsjet im Farbdoppler
- paradoxerweise bei akuten Klappeninsuffizienzen im Farbdoppler oft nur geringgradig imponierender Jet
- Gefahr der Unterschätzung des Schweregrades im Farbdoppler
- bei noch nicht dilatiertem kleinem linkem Ventrikel unterschätzte Jetfläche
- tachykardiebedingte kurze Regurgitationszeit
- schlechte zeitliche Auflösung des Farbdopplers
- Graduierung mittels Messung der Vena contracta
- erhöhte Pixeldichte des Flussignals bei schwergradiger MV-Insuffizienz
Zoghbi WA (2003) J Am Soc Echocardiogr 16:777-802
MV-Insuffizienz
MV-Insuffizienz III° bei 56 jährigen, trainierten Mann mit seit ca. 2 Wochen bestehender Dyspnoe und jetzt kardialem Lungenödem.
pragmatisches Vorgehen
nach Ausschluss anderer Ursachen bei bisher nicht bekanntem Vitium und typischer Klinik bei Darstellung eines Regurgitationsjets und erhaltener LV-EF von akut aufgetretener, relevanter Klappeninsuffizienz als Ursache der hämodynamischen Instabilität ausgehen
hämodynamisches Monitoring
hämodynamisches Monitoring
- mittels Echokardiographie adaequat noninvasiv durchzuführen
- im Falle eines komplizierten oder refraktären Schocks dem Rechtsherzkatheter/ PiCCO an brauchbaren Informationen überlegen, ermöglicht jedoch kein kontinuierliches Monitoring
- gute Korrelation invasiv vs. noninvasiv
- mehr zur Verlaufsbeurteilung als für Erhebung präziser einzelner Werte
- zusätzliche Informationen (kompromittierender Perikarderguss etc.)
Mayo P (2015) Intensive Care Med 41(6):1103-1106
Messung des HZV
Voraussetzung für die echokardiographische Bestimmung des Herzzeitvolumens ist die akkurate, senkrechte Anlotung des linksventrikulären Ausflusstraktes im apikalen 5-Kammerblick.
Messung des HZV
Abweichungen der Anlotung von bis zu maximal 20° sind tolerabel. Bei größeren Winkelabweichungen steigt die Ungenauigkeit der HZV-Messung ausgehend von 6% bei 20° exponentiell an.
Messung des HZV
Das Probe-Volume wird in der Mitte des LVOT etwa 5 mm oberhalb der Aortenklappenebene platziert.
Messung des HZV
Das Pulsed-wave-Doppler (pw)-Signal lässt erkennen, mit welcher Geschwindigkeit (v = m/s) das Blut zum jeweiligen Zeitpunkt befördert wird.
Messung des HZV
Das Multiplikation des Velocity time integral mit der LVOT-Querschnittsfläche [π (LVOT/2)2] ergibt das Schlagvolumen.
Das Multiplikation des Velocity time integral mit der LVOT-Querschnittsfläche [π (LVOT/2)2] ergibt das Schlagvolumen.
Beigel R (2014) J Crit Care 29:184e1-184e8Anmerkungen zur Cardiac output-Messung
- Messung des LVOT-Durchmessers unmittelbar unterhalb Aortenklappenansatz
- Ausgangsformel: SV = π x rLVOT2 x VTILVOT
- Messung in der parasternalen Längsachse = zusätzliche Schnittebene und fehleranfällig
- LVOT statischer Wert (Normwert 18 bis 22 mm), VTI (Normwert 18 bis 22 cm)
- zur qualitativen HZV-Bestimmung Verwendung nur des VTILVOT bei erhaltener Korrelation zum HZV
- Flußbeschleunigung im Bereich des Probe-Volumes (z.B. AoV-Stenose) führt zur Überschätzung des VTILVOT
- zur qualitativen HZV-Bestimmung lediglich Berücksichtigung des VTILVOT aufgrund der extrem fehlerbehafteten LVOT-Bestimmung und der guten Korrelation des VTILVOT zum HZV
- zur exakten Bestimmung werden 3 bis 5 Messungen gemittelt
- bei Vorhofflimmern 5 bis 10 Messungen
Mayo P (2015) Intensive Care Med 41(6):1103-1106
Volumenstatus II
dynamische echokardiographische Parameter
- VTILVOT-Schwankungen unter Atmung/ Passive leg raising: Volumengabe!
- Anstieg des VTILVOT unter 250 ml Volumen-Bolus: Volumengabe!
erweiterte Therapiesteuerung anhand der VTILVOT
- Inotropikasupport
- Gabe von Dobutamin, 3 min. später Kontrolle der VTI und ggf. weiterer Steigerung des Dobutamins

... wie geht es weiter?

European Diploma in Advanced Critical Care EchoCardiography